Una grave miosite che mima la sindrome di Guillain-Barré: un caso di interazione tra statina e acido bempedoico
Pietro Tito Ugolotti1, MD; Davide Donelli1, MD; Gianluca Signoretta1, MD; Nicola De Santis1, MD; Giampaolo Niccoli1, MD
1. Cardiology Division, Azienda Ospedaliero-Universitaria di Parma, Viale Antonio Gramsci, 14, 43126 Parma (PR), Italy
Abstract
I pazienti anziani si caratterizzano per un esponenziale incremento della fragilità, legata sia all’aumentato rischio cardiovascolare sia a specifiche comorbidità che si amplificano a vicenda, spesso limitando le scelte terapeutiche e con la necessità di una poli-farmacoterapia, in prevenzione cardiovascolare primaria e secondaria, di cui spesso sfugge il quadro di insieme. In questo caso clinico presentiamo una paziente con nota cardiopatia ischemica cronica postinfartuale, severa disfunzione ventricolare sinistra nonostante terapia medica ottimizzata, con insufficienza renale cronica in stadio IV, deceduta a seguito di una grave rabdomiolisi imputabile a una possibile interazione sfavorevole tra acido bempedoico e atorvastatina.
Caso clinico
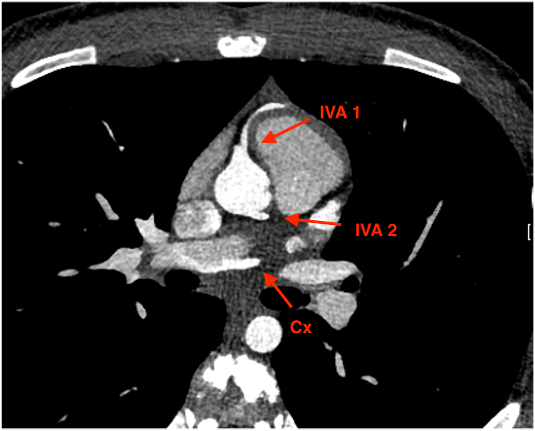
La protagonista del nostro caso clinico è una donna di 83 anni affetta da ipertensione arteriosa, ipercolesterolemia, diabete mellito tipo 2 e insufficienza renale cronica (IRC) multifattoriale (eGFR 29 ml/min: stadio IV). Si segnala inoltre una cardiopatia ischemica cronica post-infartuale: nel 2017 aveva avuto una sindrome coronarica acuta senza sopraslivellamento del tratto ST (SCA-NSTEMI) con occlusione totale cronica dell’arteria interventricolare anteriore (IVA, trattata con posizionamento di quattro stent medicati), con grave riduzione della frazione di eiezione (FE 27%). Nel 2018 era stato impiantato un dispositivo di resincronizzazione cardiaca con defibrillatore impiantabile (CRT-D) in prevenzione primaria. Nel 2021 si era verificata una recidiva di infarto miocardico con riscontro di occlusione totale intrastent, gestita conservativamente. La paziente era stata dimessa in cardioaspirina+ ticagrelor, insieme ad atorvastatina 80 mg ed ezetimibe. A causa del quadro di malattia renale cronica, non vi era stata alcuna possibilità di titolare la terapia specifica per l’insufficienza cardiaca (ACE inibitore/sartano/entresto, antagonista del recettore dei mineralcorticoidi , SGLT2-inibitore) maggiore di ramipril 1,25 mg/die.
Ai controlli si docuementava miglioramento della FE (40% circa).
Nel 2022 erano stati rilevati livelli persistentemente elevati dei marker epatici con riscontro di moderata steatofibrosi epatica, attribuita all’uso di atorvastatina 80 mg, successivamente regredita con riduzione del dosaggio a 20 mg.
L’anno successivo la paziente presentò una recidiva di infarto imputata alla nota occlusione cronica dell’IVA, con indicazione a sola terapia medica, e con una residua FE del 28%. La terapia ipolipemizzante era stata implementata con atorvastatina 80 mg ed ezetimibe.
Nei mesi successivi, considerata l’ipercolesterolemia residua (LDL-c pari a 101 mg/dl) è stato iniziato acido bempedoico 80 mg. La restante terapia includeva: cardioaspirina, clopidogrel, furosemide 25 mg, metoprololo 100 mg ½ cp due volte al giorno, omega-3, terapia insulinica. Dopo pochi giorni, la paziente ha sviluppato un’infezione urinaria da Klebsiella Pneumoniae per cui veniva avviata ciprofloxacina. Nei giorni successivi il quadro clinico è peggiorato, con comparsa di gravi dolori agli arti inferiori, danno renale acuto e incremento dell’uricemia. La successiva comparsa di tosse e il progressivo peggioramento dell’ipostenia agli arti inferiori hanno portato la paziente ad effettuare un accesso in Pronto Soccorso (PS). Qui la paziente si presentava in compenso emodinamico, con marcata leucocitosi neutrofila, significativo aumento della PCR ma procalcitonina negativa, funzionalità renale stabile (creatininemia 1,9 mg/dl), significativo rialzo delle transaminasi (ALT 771 U/L); BNP e hs-TnI solo lievemente elevati.
Nel sospetto di uro-sepsi si procedeva al ricovero in Geriatria, con miglioramento degli indici di flogosi all’introduzione del Meropenem. La paziente aveva però sviluppato disartria, immobilità palatale e disfagia, con significativo deficit nella flessione della testa, ipostenia prossimale degli arti superiori con caduta immediata durante Mingazzini. Tali elementi e il contestuale riscontro di un livello di CPK pari a 15.450 U/L, hanno portato il neurologo a sospettare una sindrome di Guillain-Barré (variante AMAN) con possibile quadro di miosite. E’ stata quindi avviata terapia immunoglobulinica ed è stata eseguita un’elettromiografia che ha rilevato segni di sofferenza miogenica e necrosi muscolare come da miosite.
Gli ulteriori esami di laboratorio hanno evidenziato: urea 257 mg/dl, creatinina 3 mg/dl, AST 1.199 U/L, ALT 746 U/L, LDH 962 U/L, CPK 16.858 U/L. Il ricovero in terapia intensiva e la dialisi sono stati ritenuti controindicati dagli specialisti interpellati.
Tre giorni dopo la sua presentazione in PS, la paziente ha sviluppato un’insufficienza respiratoria acuta con successivo arresto cardiaco che ha causato la morte della paziente.
Discussione
Secondo le ultime linee guida ESC1, i pazienti con rischio cardiovascolare molto elevato dovrebbero mantenere i livelli di LDL-c al di sotto di 40 mg/dl. Nonostante la paziente del caso assumesse la dose massima tollerata di statina e di ezetimibe, tale target non era stato raggiunto. Nonostante la storia di steatofibrosi attribuibile alle statine, dopo la seconda SCA la paziente era stata dimessa con atorvastatina 80 mg in prevenzione secondaria. Secondo l’ Agenzia Italiana del Farmaco (AIFA), gli inibitori del PCSK9 non sono raccomandati oltre gli 80 anni2, così dopo la terza sindrome coronarica acuta, l’acido bempedoico è stato introdotto come ultima risorsa per abbassare i livelli di LDL-c.
Nel nostro caso clinico, la grave miosite potrebbe essere attribuita ad un meccanismo multifattoriale che coinvolge la tossicità muscolare diretta da statine e acido bempedoico, la ridotta clearance del farmaco dovuta all’ insufficienza renale e una possibile suscettibilità idiopatica.
Le statine possono causare una miopatia, che può andare da una lieve mialgia fino alla rabdomiolisi, mentre sono diversi i passaggi molecolari coinvolti. 3
L’acido bempedoico inibisce la sintesi del colesterolo agendo sull’ATP citrato liasi, a monte della HMG-coA reduttasi 4. Tale molecola viene attivata nel fegato e si ritiene abbia un minor rischio di danni muscolari perché non attivo nel muscolo scheletrico. Tuttavia, se usato in combinazione con le statine, il rischio di lesioni muscolari potrebbe aumentare per effetti additivi ancora parzialmente ignoti.
L’inclusione dell’acido bempedoico nelle Linee Guida Europee permette il suo utilizzo nei pazienti con effetti avversi muscolo-scheletrici delle statine, che colpiscono tra il 7 e il 29% dei pazienti, la cui non titolazione determina una riduzione insufficiente delle LDL 5-6-7. Nello studio di approvazione per l’acido bempedoico, solo il 22,9% dei pazienti ha ricevuto il farmaco associato a statina. Ci sono stati solo due casi di rabdomiolisi, senza differenze significative rispetto al placebo8. La co-somministrazione di a. bempedoico con simvastatina o pravastatina aumenta significativamente la loro AUC e la Cmax, mentre le interazioni con atorvastatina, rosuvastatina ed ezetimibe non sono risultati significative9.
L’European Medicines Agency (EMA) e AIFA sconsigliano fortemente la co-somministrazione dell’acido bempedoico con dosi elevate di simvastatina, ma il nostro caso suggerisce che anche la combinazione con atorvastatina dovrebbe essere valutata con cautela. Pur essendo corretto raggiungere i target raccomandati, il principio del “primum non nocere” non dovrebbe mai esser dimenticato: ciò implica evitare di prescrivere combinazioni farmacologiche superficialmente, specie negli anziani. Occorre monitorare sintomi e indici di miocitonecrosi dopo l’inizio del trattamento con statine e bempedoico, oltre a condurre ulteriori ricerche per comprendere eventuali interazioni avverse.
Bibliografia
1) Byrne, Robert A., Xavier Rossello, J. J. Coughlan, Emanuele Barbato, Colin Berry, Alaide Chieffo, Marc J. Claeys, et al. 2023. “2023 ESC Guidelines for the Management of Acute Coronary Syndromes.” European Heart Journal 44 (38): 3720–3826.
2) Di Fusco, Stefania Angela, Stefano Aquilani, Antonella Spinelli, Alessandro Alonzo, Lorenzo Castello, Pasquale Caldarola, Leonardo De Luca, et al. 2023. “[ANMCO Expert opinion: Bempedoic acid place in therapy for hypercholesterolemia management].” Giornale italiano di cardiologia 24 (6): 490–98.
3) Di Stasi, Stephanie L., Toran D. MacLeod, Joshua D. Winters, and Stuart A. Binder-Macleod. 2010. “Effects of Statins on Skeletal Muscle: A Perspective for Physical Therapists.” Physical Therapy 90 (10): 1530–42.
4) Pinkosky, Stephen L., Roger S. Newton, Emily A. Day, Rebecca J. Ford, Sarka Lhotak, Richard C. Austin, Carolyn M. Birch, et al. 2016. “Liver-Specific ATP-Citrate Lyase Inhibition by Bempedoic Acid Decreases LDL-C and Attenuates Atherosclerosis.” Nature Communications 7 (November): 13457.
5)Bytyçi, Ibadete, Peter E. Penson, Dimitri P. Mikhailidis, Nathan D. Wong, Adrian V. Hernandez, Amirhossein Sahebkar, Paul D. Thompson, et al. 2022. “Prevalence of Statin Intolerance: A Meta-Analysis.” European Heart Journal 43 (34): 3213–23.
6) Hovingh, G. Kees, Shravanthi R. Gandra, Jan McKendrick, Ricardo Dent, Heather Wieffer, Alberico L. Catapano, Paul Oh, Robert S. Rosenson, and Erik S. Stroes. 2016. “Identification and Management of Patients with Statin-Associated Symptoms in Clinical Practice: A Clinician Survey.” Atherosclerosis 245 (February): 111–17.
7) Stroes, Erik S., Paul D. Thompson, Alberto Corsini, Georgirene D. Vladutiu, Frederick J. Raal, Kausik K. Ray, Michael Roden, et al. 2015. “Statin-Associated Muscle Symptoms: Impact on Statin Therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management.” European Heart Journal 36 (17): 1012–22.
8) Halsey, Grace. 2022. “Bempedoic Acid Meets Primary Endpoint in Key Cardiovascular Outcomes Trial: CLEAR,” December 8, 2022.
9) Biolo, Gianni, Pierandrea Vinci, Alessandro Mangogna, Matteo Landolfo, Paolo Schincariol, Nicola Fiotti, Filippo Mearelli, and Filippo Giorgio Di Girolamo. 2022. “Mechanism of Action and Therapeutic Use of Bempedoic Acid in Atherosclerosis and Metabolic Syndrome.” Frontiers in Cardiovascular Medicine 9 (October): 1028355.


Related Posts