UNO STRANO CASO DI MALATTIA ARITMOGENA AD INTERESSAMENTO BIVENTRICOLARE…O FORSE NO?
Dott.ssa Antonella Accietto, Dott.ssa Maria Francesca Scuppa, Dott. Francesco Chietera, Dott. Mattia Garofalo, Dott.ssa Anna Corsini, Dott. Mario Sabatino, Prof. Carmine Pizzi
Alma Mater Studiorum Università di Bologna
IRCCS Azienda Ospedaliero-Universitaria di Bologna – Policlinico di Sant’Orsola
ABSTRACT
Presentiamo il caso di un paziente di 49 anni, senza comorbidità, con segni e sintomi di scompenso cardiaco acuto complicato da instabilità aritmica ed emodinamica. La severità del quadro clinico è rispecchiata dal quadro strumentale, con elementi di marcata patologia, quasi patognomonici, sia all’ECG che all’ecocardiogramma che alla risonanza magnetica cardiaca. Il sospetto diagnostico di sarcoidosi viene confermato dalla PET e dalla biopsia endomiocardica. Peculiarmente l’interessamento è esclusivamente cardiaco. Grazie alla terapia antiaritmica, alla terapia farmacologica e meccanica dello scompenso cardiaco e alla terapia immunosoppressiva, il paziente supera la fase acuta per andare successivamente incontro a trapianto cardiaco.
CASO CLINICO
Un uomo di 49 anni eseguiva una valutazione cardiologica ambulatoriale presso altro centro per astenia e dispnea da sforzo ingravescente presenti da alcune settimane. Il paziente, ciclista amatoriale, non riferiva alcuna comorbidità di rilievo, antecedenti cardiologici o fattori di rischio cardiovascolare, inclusa familiarità per cardiopatia o morte improvvisa. L’ECG (Fig. 1) mostrava un ritmo sinusale con complessi QRS larghi e frammentati, inclusa un’evidente onda epsilon; un precedente tracciato, eseguito tre anni prima, risultava invece completamente nella norma. All’ecocardiogramma si evidenziava una dilatazione e disfunzione biventricolare, moderate a sinistra e lievi a destra, in assenza di valvulopatie maggiori o versamento pericardico.
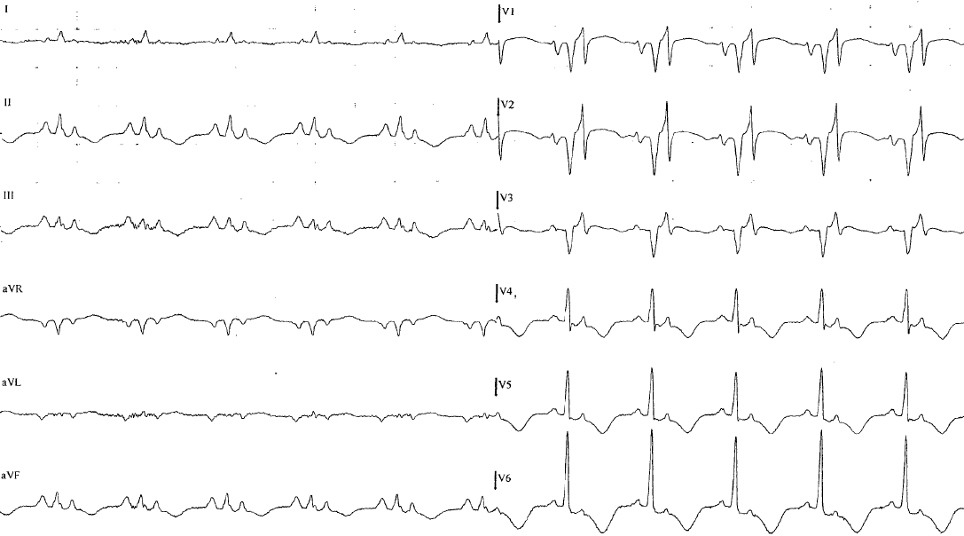
Fig.1 ECG 12 derivazioni: ritmo sinusale con complessi QRS larghi e frammentati, inclusa un’evidente onda epsilon.
Si procedeva pertanto ad esecuzione di coronarografia, con riscontro di arterie coronarie indenni, e di RM cardiaca (Fig.2), che rivelava la presenza di diffuso danno miocellulare/interstiziale associato ad edema e a late gadolinium enhancement intramiocardico, con esteso coinvolgimento biventricolare (pattern ring-like). Alla luce di questi dati, veniva posto il sospetto diagnostico di cardiomiopatia aritmogena ad interessamento biventricolare, intrapresa bassa dose di beta-bloccante ed ACE-inibitore e programmato ricovero elettivo per impianto di defibrillatore (ICD) in prevenzione primaria.
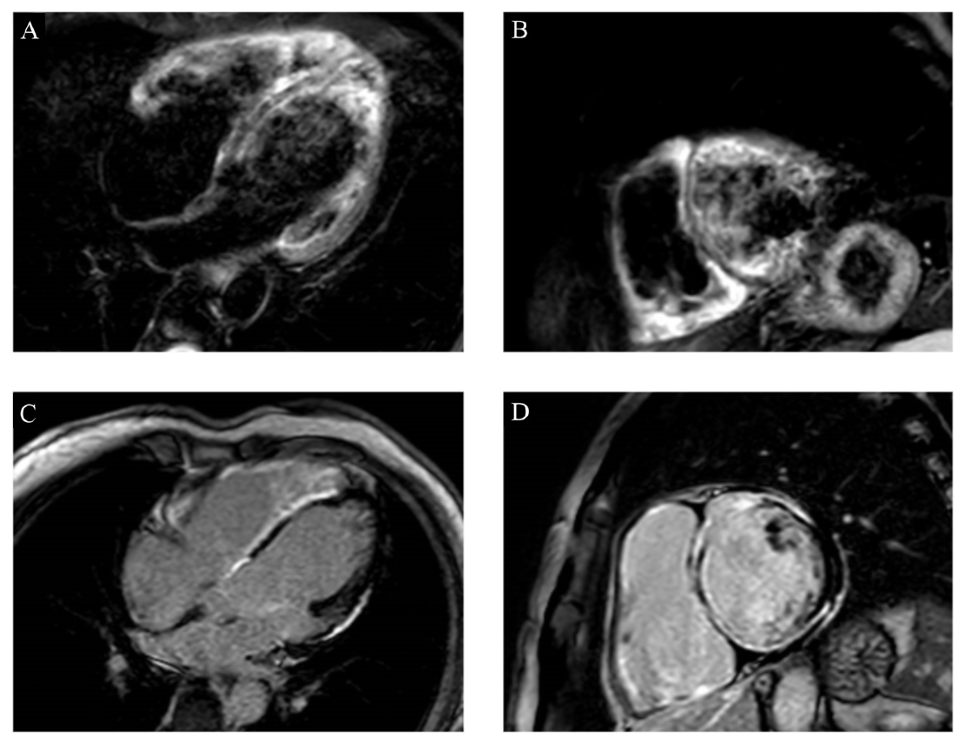
Fig.2 Risonanza magnetica cardiaca con gadolinio: A) e B) immagini T2-pesate in asse lungo e asse corto con evidenza di edema biventricolare diffuso. C) e D) immagini acquisite tardivamente dopo somministrazione intravenosa di gadolinio con evidenza di late gadolinium enhancement (danno verosimilmente fibrotico) intramiocardico biventricolare diffuso, con pattern ring-like (risparmio della sola parete infero-laterale medio-apicale e dell’apice).
Al domicilio, tuttavia, le condizioni cliniche del paziente peggioravano (incremento ponderale di circa 10 kg ed ortopnea) rendendo necessario un accesso in pronto soccorso, anche a causa della comparsa di cardiopalmo. In pronto soccorso si evidenziava la presenza di una tachicardia ventricolare sostenuta (TVS) con polso, trattata efficacemente con DC-shock ma seguita da numerose recidive nonostante la terapia antiaritmica endovenosa con lidocaina ed amiodarone. Il paziente veniva quindi centralizzato presso la nostra unità di terapia intensiva cardiologica (UTIC).
All’arrivo in UTIC, data la marcata instabilità elettrica con TVS subentranti, gradualmente responsive alla procainamide, e la contestuale compromissione emodinamica con segni di bassa portata, veniva posizionato contropulsatore aortico e impostata terapia endovenosa con inotropi e diuretico. All’ecocardiogramma (Fig.3), così come alla revisione della risonanza magnetica cardiaca eseguita in precedenza, si poneva l’accento, oltre che sulla severa dilatazione e disfunzione biventricolare associata a insufficienze mitralica e tricuspidale funzionali severe, sulla presenza di un focale assottigliamento (3 mm) con discinesia del setto interventricolare medio-basale, caratteristica non frequente nella cardiomiopatia aritmogena bensì tipica della sarcoidosi cardiaca.
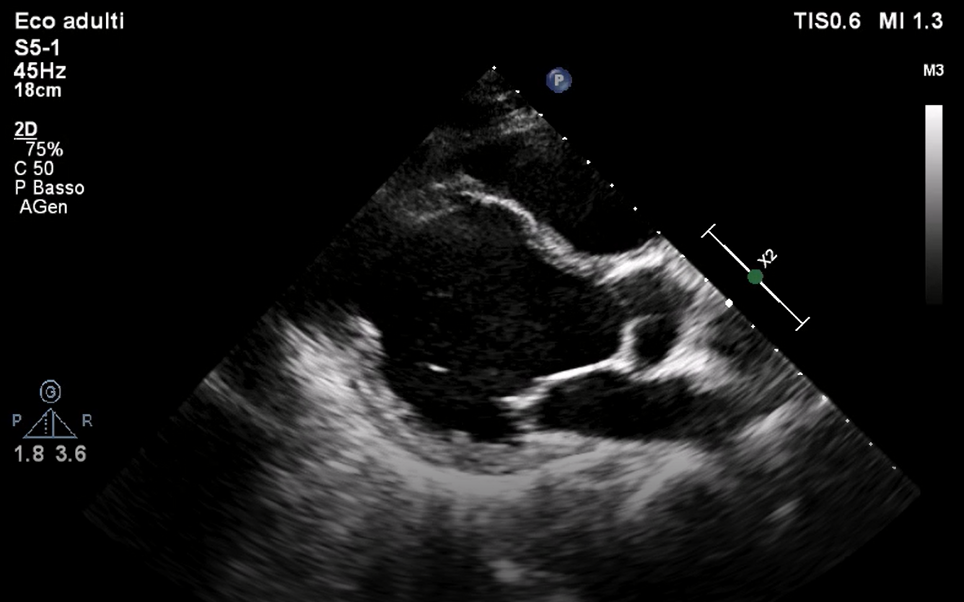
Fig.3 Ecocardiogramma: immagine in parasternale asse lungo con focus sull’estremo assottigliamento (3 mm) focale del setto interventricolare medio.
Anche la rapida progressione di malattia e l’assenza di familiarità sembravano rendere più probabile tale eziologia. In considerazione del sospetto diagnostico, nonché dell’instabilità elettrica ed emodinamica, veniva quindi eseguita una biopsia endomiocardica (BEM), la quale evidenziava la presenza di aree di infiammazione attiva con granulomi non necrotizzanti alternati a fibrosi subendocardica ed interstiziale: quadro compatibile con sarcoidosi cardiaca. La PET con 18-fluoro-2-desossiglucosio rilevava un’ipercaptazione cardiaca diffusa, mentre la TC total body, la RM cerebrale, l’esame del fundus oculi e una valutazione dermatologica escludevano la presenza di coinvolgimento extra-cardiaco. I livelli sierici dell’enzima di conversione dell’angiotensina (ACE) risultavano nella norma.
In considerazione della diagnosi di sarcoidosi cardiaca isolata veniva intrapresa terapia corticosteroidea endovenosa ad alto dosaggio con iniziale apparente beneficio in termini di burden aritmico. Tuttavia, in seguito ad una ulteriore recidiva di TVS nonostante la terapia immunosoppressiva e la terapia medica dello scompenso cardiaco acuto, gradualmente introdotta e titolata, si associava terapia con amiodarone, con beneficio. Ad un mese dall’inizio della terapia corticosteroidea veniva ripetuta una RM cardiaca, la quale tuttavia non mostrava alcun miglioramento del coinvolgimento biventricolare. Si procedeva pertanto a potenziamento della terapia immunosoppressiva con aggiunta di metotrexato, in associazione a corticosteroide a dosaggio di mantenimento per os, con successiva dimostrazione istologica di parziale risoluzione dell’infiammazione granulomatosa ad una BEM di controllo. Nel corso del ricovero si procedeva inoltre ad impianto di ICD transvenoso in prevenzione secondaria. Veniva inoltre eseguito, in condizioni di ottimale compenso cardiocircolatorio, un cateterismo cardiaco destro che mostrava un basso indice cardiaco a riposo a fronte di resistenze polmonari nei limiti di norma, per cui, alla luce del quadro complessivo, il paziente veniva inserito in lista d’attesa per trapianto di cuore, e infine dimesso.
Sfortunatamente, nonostante la terapia medica, tre mesi dopo la dimissione seguiva un nuovo ricovero per recidiva di TVS, efficacemente trattata dall’ICD. Il paziente andava incontro a trapianto di cuore circa 3 mesi dopo, in assenza di complicanze.
DISCUSSIONE
La sarcoidosi è una patologia granulomatosa multisistemica ad eziologia non nota, verosimilmente immuno-mediata.1 E’ presente interessamento polmonare nel 95% dei casi, seguito da quello cutaneo (16%), linfonodale ed epatosplenico, mentre quello cardiaco è molto più raro (2-3%) anche se potenzialmente sottostimato (fino a 25% in termini di riscontro autoptico); la fibrosi polmonare può generare ipertensione polmonare di gruppo 3.2 Non esiste un test diagnostico specifico: piuttosto la diagnosi richiede un quadro clinico-radiologico compatibile, l’esclusione di diagnosi alternative e la conferma istologica di granulomi non-caseosi.3 A tal proposito l’ACE, prodotto dai granulomi, è elevato solo nel 75% dei casi, con peraltro una bassa specificità.4 La maggior parte dei pazienti raggiunge la remissione completa della malattia entro 10 anni senza richiedere alcuna terapia; un terzo dei pazienti invece manifesta compromissione organica strutturale e/o funzionale, con una mortalità complessiva del 5% dovuta a cause respiratorie, neurologiche o cardiache (disfunzione ventricolare, blocchi atrio-ventricolari e tachiaritmie ventricolari sino alla morte improvvisa), per cui in tali pazienti è indicata terapia corticosteroidea da rivalutare nel corso dei mesi/anni successivi.1 Il metotrexato è l’unico farmaco di seconda linea studiato, utile come strategia steroid-sparing. I pazienti con sarcoidosi cardiaca che necessitano di trapianto di cuore hanno una sopravvivenza a breve e medio termine maggiore rispetto a quelli che ne necessitano per altre cause.6
Nell’ambito della diagnosi differenziale della cardiopatia a fenotipo dilatativo, la sarcoidosi è una diagnosi non comune, né semplice. L’ECG, il severo interessamento biventricolare e l’espressione aritmica possono, come nel nostro caso, inizialmente orientare verso la ormai più comunemente attenzionata cardiomiopatia aritmogena, nonché verso altre eziologie, specialmente ad impronta genetica. Tuttavia, l’assenza di familiarità e la rapida progressione della malattia hanno smorzato tale ipotesi, e insieme al marcato interessamento del setto interventricolare, spesso estremamente assottigliato, hanno modificato l’orientamento diagnostico, seppur in assenza di interessamento polmonare; l’indagine di terzo livello (BEM) si è pertanto resa necessaria per via della potenziale reversibilità della patologia sarcoidotica.1
BIBLIOGRAFIA
1) Iannuzzi MC, Rybicki BA, Teirstein AS. Sarcoidosis. N Engl J Med. 2007 Nov 22;357(21):2153-65.
2) Baughman RP, Teirstein AS, Judson MA, Rossman MD, Yeager H Jr, Bresnitz EA, DePalo L, Hunninghake G, Iannuzzi MC, Johns CJ, McLennan G, Moller DR, Newman LS, Rabin DL, Rose C, Rybicki B, Weinberger SE, Terrin ML, Knatterud GL, Cherniak R; Case Control Etiologic Study of Sarcoidosis (ACCESS) research group. Clinical characteristics of patients in a case control study of sarcoidosis. Am J Respir Crit Care Med. 2001 Nov 15;164(10 Pt 1):1885-9.
3) Statement on sarcoidosis. Joint Statement of the American Thoracic Society (ATS), the European Respiratory Society (ERS) and the World Association of Sarcoidosis and Other Granulomatous Disorders (WASOG) adopted by the ATS Board of Directors and by the ERS Executive Committee, February 1999. Am J Respir Crit Care Med. 1999 Aug;160(2):736-55.
4) Ungprasert P, Carmona EM, Crowson CS, Matteson EL. Diagnostic Utility of Angiotensin-Converting Enzyme in Sarcoidosis: A Population-Based Study. Lung. 2016 Feb;194(1):91-5.
5) Baughman RP, Winget DB, Lower EE. Methotrexate is steroid sparing in acute sarcoidosis: results of a double blind, randomized trial. Sarcoidosis Vasc Diffuse Lung Dis. 2000 Mar;17(1):60-6.
6) 2006 Annual report of the U.S. Organ Procurement and Transplantation Network and the Scientific Registry of Transplant Recipients. Rockville, MD: United Network for Organ Sharing, 2006.



Related Posts