I.Pagliassotto1;2; M.Brero1;2; G.Giannino1;2; M.Bellettini1; F.Angelini1; S.Frea1; Prof. G.M. De Ferrari1;2
Division of Cardiology, AOU Città della Salute e della Scienza, Turin; Department of Medical Sciences, University of Turin
Abstract
La miocardite da immunocheckpoint-inibitori (ICI) è un evento raro connesso alla terapia, con incidenza descritta fino al 2%. Presentiamo il caso di un uomo in terapia con pembrolizumab, che ha sviluppato miocardite da ICI esordita con shock cardiogeno e complicata da eventi aritmici e vasospasmo coronarico. In queste forme severe la mortalità si attesta intorno al 40% e la diagnosi precoce e il trattamento mirato sono cruciali per migliorare l’outcome.
Background
Da circa vent’anni gli ICI si sono affacciati nel panorama delle terapie oncologiche mirate; tra essi trovano spazio gli inibitori di PD1, proteina della morte cellulare programmata, espressa sulla superficie del linfocita T, che agiscono favorendo la risposta infiammatoria contro la cellula neoplastica1. Tale terapia talora comporta effetti avversi cardiovascolari potenzialmente fatali.
Case presentation
Un uomo di 68 anni, senza precedenti cardiologici, in terapia con pembrolizumab per un carcinoma uroteliale recentemente recidivato, accedeva in DEA per insorgenza da alcuni giorni di dispnea e ortopnea. All’arrivo si presentava con quadro di shock cardiogeno SCAI C (lattati 4.2 mmol/L), con danno d’organo epatico e renale (AST/ALT 624/858 UI/L, creatinina 1.72 mg/dl), segni di flogosi acuta (PCR 102 mg/dl), aumento del NTproBNP (5760 ng/dl) e lieve movimento troponinico (TnI 49 – 55 ng/dl). L’ECG non mostrava anomalie significative, mentre all’ecoscopia si dimostrava una severa disfunzione ventricolare sinistra (LVEF 10%) in presenza di ipocinesia diffusa. Ricoverato in UTIC, avviava Dobutamina 5 mcg/kg/min, nitroprussiato e furosemide in infusione continua con buona risposta clinico-laboratoristica. Alla luce del quadro di presentazione in paziente con plurimi fattori di rischio cardiovascolare ed elevata probabilità pre-test di malattia coronarica, a miglioramento del compenso veniva eseguita la coronarografia, che mostrava lesioni angiograficamente subcritiche (70%) della coronaria destra, non sottoposte ad angioplastica. Il contestuale cateterismo cardiaco destro in terapia (dobutamina e nitroprussiato) mostrava normale regime pressorio polmonare (PAP 25/10/15 mmHg, PCWP 10 mmHg) e portata cardiaca severamente ridotta (CI 1.7 L/min/m2), e veniva infine eseguita biopsia endomiocardica che mostrava infiltrato infiammatorio ricco di linfociti T compatibile con miocardite acuta. Come da protocollo interno, eseguiti screening infettivo e autoimmune risultati negativi. In considerazione dell’elevata probabilità di diagnosi di miocardite da ICI, veniva avviata terapia steroidea con Metilprednisolone 1g/die, sostituito in quarta giornata con Prednisone 1 mg/kg/die, con rapido miglioramento clinico. Alla RMN cuore eseguita in IV giornata, evidenza di valori di T1 nativo elevati, in assenza di diffuso LGE, per cui si confermava il sospetto diagnostico di miocardite. In V giornata di ricovero, III giornata post terapia steroidea ad alto dosaggio, in assenza di segni di peggioramento del compenso o disionie, il paziente andava incontro ad arresto cardiocircolatorio in blocco atrioventricolare avanzato con necessità di manovre rianimatorie e ROSC a 1 minuto. Eseguita coronarografia in emergenza che escludeva instabilità di placca sulla coronaria destra, e veniva posizionato un pacemaker temporaneo, rimosso quattro giorni dopo per assenza di recidive bradiaritmiche. Contestualmente si ripeteva bolo di Metilprednisolone 500 mg ev ed avviava Micofenolato Mofetile. In VII giornata, per comparsa di angor e sopraST inferiore, veniva ripetuta coronarografia: alla valutazione IVUS coronaria destra prossimale con MLA critica, per cui eseguita angioplastica con stenting. Nei giorni successivi si susseguivano diversi episodi analoghi caratterizzati da angor con sopraST transitorio, a regressione spontanea nell’arco di minuti, associati ad importante reazione vagale, di non univoca interpretazione (trigger vs reazione vagale per riflesso di Bezold-Jarish). La breve durata e risoluzione spontanea degli eventi, anche documentati all’ECG-Holter-12D (Figura), permetteva di ipotizzare, vista l’assente documentazione angiografica, un vasospasmo coronarico. Inoltre, la prevalenza notturna e post prandiale non preceduta da malessere, indirizzava verso un trigger vagale. Nonostante la FE ridotta si rendeva necessario l’avvio di Verapamil endovena per inefficacia della sola nitroglicerina nel controllo degli eventi, e si avviava Tiotropio bromuro inalatorio off-label per ridurre il trigger vagale, con immediato beneficio e senza ulteriori episodi vasospastici. Nel successivo decorso il paziente si è mantenuto stabile, con recupero parziale della funzione sistolica (LVEF 47%) e switch a terapia orale, mantenendo terapia eziologica immunosoppressiva in dimissione.
Discussione e conclusioni
Tra gli effetti avversi cardiovascolari degli ICI la miocardite rappresenta un evento raro: l’incidenza è intorno al 2%, e aumenta al 17% nei pazienti in terapia combinata2. L’esatta patogenesi non è chiara, ma sembrerebbe correlata all’espressione cardiomiocitaria di PDL1, con conseguente reazione autoinfiammatoria3,4. La mortalità è, nelle forme severe, del 40%, pertanto una disamina completa cardiologica è fondamentale per la diagnosi precoce. La RMN cuore permette una precisa caratterizzazione tissutale con elevata accuratezza diagnostica delle sequenze T1-pesate3, ma il gold standard è rappresentato dalle biopsie endomiocardiche, con ricco infiltrato di linfociti T. La terapia della miocardite da ICI prevede, dopo l’interruzione dell’agente responsabile, steroide ad alta dose seguito, se inefficace, da immunosoppressori di seconda linea6. In casi di miocardite fulminante è stata proposta anche la possibilità di terapia con plasmaferesi. Le complicanze aritmiche sono rare, ma con significativa correlazione tra l’assunzione di pembrolizumab e la comparsa di blocchi atrioventricolari4. Pochi sono i casi di vasospasmo descritti in questa popolazione di pazienti5,6, per verosimile trigger autoinfiammatorio sull’endotelio coronarico, ma ulteriori studi sono necessari per comprenderne meglio la patogenesi e la gestione terapeutica in acuto e durante il follow-up.
References
1 Varricchi, Gilda et al. “Cardiotoxicity of immune checkpoint inhibitors.” ESMO open vol. 2,4 e000247. 26 Oct. 2017, doi:10.1136/esmoopen-2017-000247
2 Moslehi, Javid et al. “Immune checkpoint inhibitor-associated myocarditis: manifestations and mechanisms.” The Journal of clinical investigation vol. 131,5 (2021): e145186. doi:10.1172/JCI145186
3 Thavendiranathan, Paaladinesh et al. “Myocardial T1 and T2 Mapping by Magnetic Resonance in Patients With Immune Checkpoint Inhibitor-Associated Myocarditis.” Journal of the American College of Cardiology vol. 77,12 (2021): 1503-1516. doi:10.1016/j.jacc.2021.01.050
4 Liu, Yunwei et al. “Arrhythmic events associated with immune checkpoint inhibitors therapy: A real-world study based on the Food and Drug Administration Adverse Event Reporting System database.” Cancer medicine vol. 12,6 (2023): 6637-6648. doi:10.1002/cam4.5438
5 Otsu, Kazuya et al. “Vasospastic angina following immune checkpoint blockade.” European heart journal vol. 41,17 (2020): 1702. doi:10.1093/eurheartj/ehz796
6 Guo, Kai et al. “PD-1 Inhibitor-Induced Thyrotoxicosis Associated with Coronary Artery Spasm and Ventricular Tachycardia.” Cardiovascular toxicology vol. 22,10-11 (2022): 892-897. doi:10.1007/s12012-022-09756-4
FIGURE
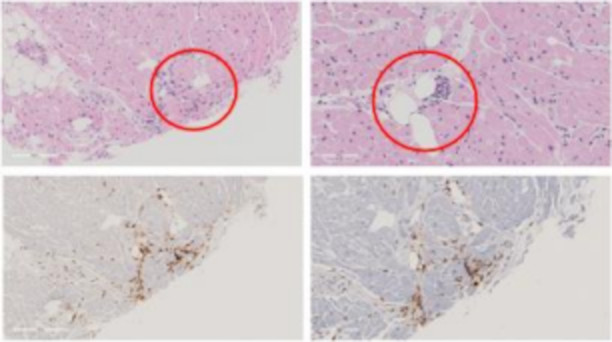
Figura 1: biopsie endomiocardiche con infiltrati T-cellulari in ematossilina-eosina e all’analisi immunoistochimica
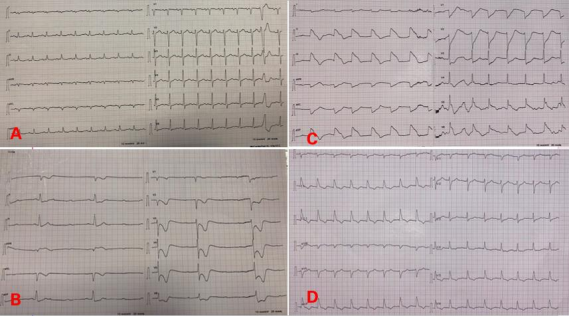
Figura 2: Tracciati ECG: A) tracciato ECG all’ingresso; B) tracciato ECG post-ROSC; C) sopraST inferiore con aspetto shark-fin in corso di vasospasmo; D) tracciato ECG al termine dell’episodio di vasospasmo
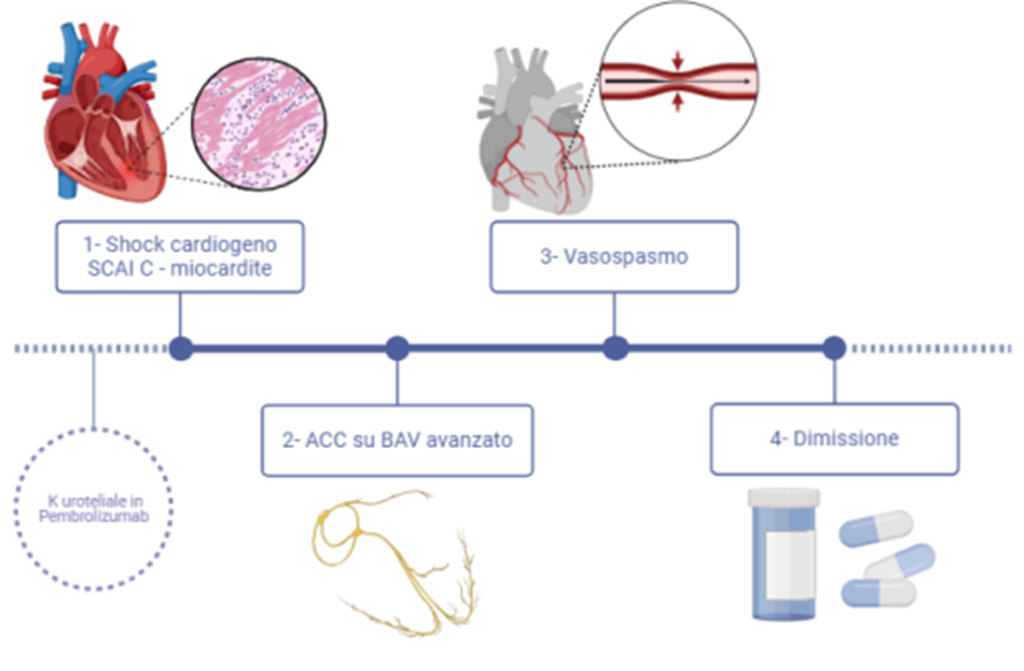
Figura 3: Timeline degli eventi: 1) esordio della miocardite ICI-relata con shock cardiogeno SCAI C, 2) arresto cardiaco su BAV avanzato, 3) episodi d vasospasmo subentranti, 4) dimissione.
