Un singolare caso di severa disfunzione ventricolare sinistra: “Breaking Bad” alla milanese
Donisi Luca 1,2, Guareschi Alessandro 1,2, Calcagnino Margherita 2, Gherbesi Elisa 2, Garascia Andrea3, Faggiano Andrea 1,2, Vicenzi Marco 1,2, Carugo Stefano 1,2
1 Department of Clinical Sciences and Community Health, University of Milano, Italy
2 Department of Cardio-Thoracic-Vascular Diseases, Foundation IRCCS Ca’ Granda Ospedale Maggiore Policlinico, Italy
3 “De Gasperis” Cardio Center, Niguarda Hospital, ASST Grande Ospedale Metropolitano Niguarda, Piazza Ospedale Maggiore, 3, 20162 Milan, Italy
ABSTRACT
In un uomo di 39 anni di origini filippine e un’anamnesi dimostratasi successivamente incompleta con nuovo riscontro di severa cardiopatia ipocinetica dilatativa veniva indagata l’eziologia mediante l’esecuzione di risonanza magnetica cardiaca, PET-TC, angio-TC coronarica, angiografia coronarica e biopsia endomiocardica con riscontro di verosimile methamphetamine-associated cardiomyopathy in overlap con un quadro di coronaropatia trivasale critica.
CASO CLINICO
Il protagonista del caso clinico è un uomo di 39 anni di origini filippine che si presentava in Pronto Soccorso per un primo riscontro di dispnea ed edemizzazione declive da circa una settimana. Dall’anamnesi raccolta si evinceva la presenza di plurimi fattori di rischio cardiovascolare: diabete mellito di tipo 2, storia pregressa di abuso alcolico (5 UI/die fino a due anni prima), steatosi epatica e fumo attivo.
Il primo elettrocardiogramma non mostrava significative alterazioni patologiche, se non un lieve sotto-livellamento nelle derivazioni infero-laterali.
Gli esami del sangue mostravano uno stabile movimento enzimatico (Troponine T 128>78>115 ng/dl), un profilo infiammatorio fluttuante senza richiamo d’organo e una funzionalità epatica alterata. All’RX del torace si evidenziava un aumento dell’ombra cardiaca con aumento della trama vascolare.
L’ecoscopia cardiaca eseguita in PS evidenziava un ventricolo sinistro dilatato (volume telediastolico VTD: 160 ml), con spessori parietali aumentati (setto/parete posteriore 13/13 mm) ed ipocinesia diffusa condizionante una severa disfunzione biventricolare (frazione d’eiezione FE 20%, Frazione d’accorciamento 20%).
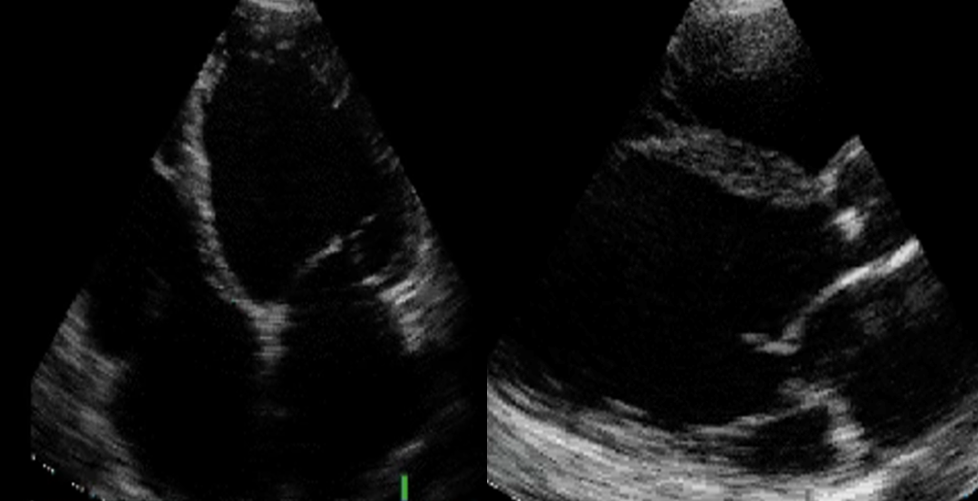
Veniva quindi posta diagnosi di scompenso cardiaco a frazione d’eiezione ridotta (HFrEF) di nuovo riscontro con indicazione a ricovero in terapia intensiva cardiologica. Durante il monitoraggio i parametri vitali si mantenevano stabili con un quadro di congestione venosa senza ipoperfusione periferica. Veniva quindi impostata terapia diuretica endovenosa con rapida risoluzione degli edemi declivi e della dispnea. A paziente stabilizzato, veniva impostata la terapia specifica per l’HFrEF.
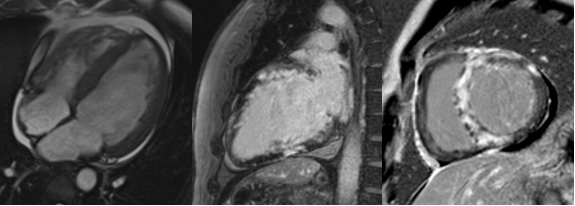
Data la giovane età e l’assenza di sintomatologia anginosa si decideva di eseguire in prima istanza la risonanza magnetica cardiaca che mostrava dimensioni aumentate del ventricolo sinistro (VTDi 112.8 ml/mq) e normali del ventricolo destro, una funzione sistolica significativamente ridotta (FE 17%), massa miocardica aumentata in presenza di diffusa ipertrofia. Inoltre, si evidenziava sia diffusa iperintensità di segnale di parete nelle sequenze STIR, con accumulo di late gadolinium enhancement (LGE) dopo somministrazione di mezzo di contrasto a carico del setto, della parete anteriore ed inferiore con aspetto patchy diffuso intramiocardico e subepicardico di significato non ischemico. Si confermava quindi un quadro di grave cardiopatia dilatativa ipocinetica con evidenza di fibrosi a distribuzione tipica di patologie infiammatorie quali la miocardite e/o la sarcoidosi.
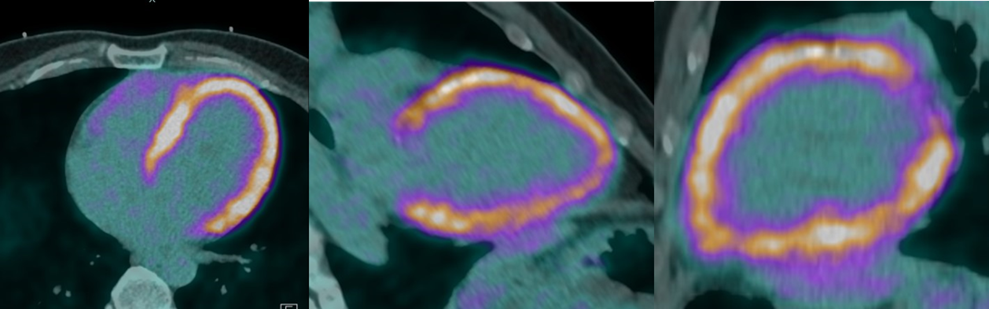
Nonostante l’assenza di aritmie, in considerazione dell’età inferiore a 40 anni e il dosaggio dell’enzima ACE positivo (81.5 U/L) si decideva, per escludere la sarcoidosi, di eseguire una PET/TC con 18- FDG la quale mostrava una diffusa ipercaptazione miocardica sinistra e moderata destra in assenza di lesioni ipercaptanti in sede extra-cardiaca. Questo aspetto era compatibile con il quadro di scompenso acuto, mentre la sarcoidosi è solitamente caratterizzata da un accumulo patchy con noduli ipercaptanti extracardiaci, per cui veniva esclusa.
Dunque, i segni clinici, elettrocardiografici e di imaging suggerivano il sospetto di miocardite acuta. Si decideva, a completamento, nonostante la bassa probabilità pre-test di cardiopatia ischemica di eseguire una angio-TC coronarica con riscontro di coronaropatia trivasale coinvolgente il tronco comune. La severità delle lesioni veniva confermata dall’angiografia coronarica.
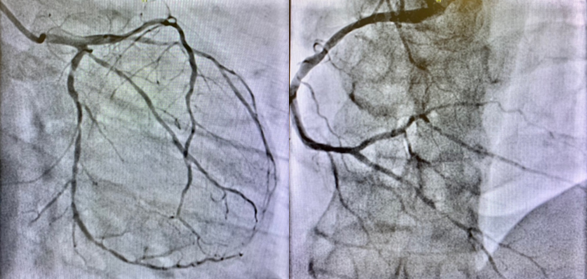
Dopo discussione in Heart Team veniva posta indicazione a bypass aortocoronarico, nonostante il quadro di coronaropatia difficilmente giustificasse il riscontro di una disfunzione ventricolare sinistra di tale entità, oltretutto caratterizzato da un pattern non-ischemico alla RM cardiaca. Pertanto, si decideva, prima di procedere a chirurgia, di eseguire una biopsia endomiocardica al fine di escludere una concomitante miocardite acuta. Il reperto anatomopatologico era privo di infiltrati infiammatori ma mostrava lieve fibrosi interstiziale senza alterazioni morfologiche dei cardiomiociti. Veniva quindi escluso anche il sospetto di miocardite acuta.
A fronte di tali riscontri di non univoca interpretazione, si decideva di effettuare una più scrupolosa anamnesi con l’aiuto di un collega psichiatria. Dal colloquio emergeva che il paziente avesse una lunga storia di abuso di shaboo, iniziata a 21 anni e sospesa solo 2 mesi prima. Lo shaboo è una droga a base di metamfetamina e caffeina particolarmente diffusa nella comunità filippina, che ha evidenziato in letteratura molteplici ripercussioni sul sistema cardiovascolare, tra cui una tossicità diretta sui miocardiociti, aumento dello stress ossidativo, disfunzione mitocondriale, vasoconstrizone polmonare e coronarica, incremento del processo aterosclerotico. L’uso cronico di queste sostanze può portare ad un quadro di severa disfunzione ventricolare che viene riconosciuto come methamphetamine-associated cardiomyopathy 1, 2, quadro compatibile con la storia del nostro paziente in cui era presente anche la cardiopatia ischemica in overlap. Il paziente veniva comunque sottoposto a rivascolarizzazione miocardica mediante duplice bypass aorto-coronarico (mammaria sinistra su interventicolare anteriore e safena su primo marginale). Dopo tre settimane di riabilitazione post-cardiochirurgia si assisteva ad un netto miglioramento del quadro ecocardiografico con normalizzazione del volume ventricolare sinistro (VTDi 80ml/mq) e solo lieve riduzione della FE (45%). A breve verrà eseguita RMN cardiaca di controllo per valutare l’eventuale miglioramento del burden di fibrosi.
CONCLUSIONI
La cardiomiopatia associata alla metanfetamina (MACM) è una condizione clinica caratterizzata da disfunzione del ventricolo sinistro e alterazioni strutturali del miocardio attribuite all’uso cronico di metanfetamine, sempre più diffuso a livello mondiale. Nell’iter diagnostico è importante soffermarsi approfonditamente sull’anamnesi perché spesso questa categoria di pazienti nasconde l’abuso di stupefacenti allo stesso staff medico che la raccoglie. Riconoscere la tossicodipendenza è fondamentale per accelerare l’iter diagnostico e impostare quanto prima la terapia adeguata per la disfunzione cardiaca sottostante. Cessare l’abuso della sostanza stupefacente rimane uno dei principali fattori prognostici in grado di favorire la reversibilità di questo tipo di cardiomiopatia3.
BIBLIOGRAFIA
[1] Kevil CG, Goeders NE, Woolard MD, Bhuiyan MS, Dominic P, Kolluru GK, Arnold CL, Traylor JG, Orr AW. Methamphetamine Use and Cardiovascular Disease. Arterioscler Thromb Vasc Biol. 2019 Sep;39(9):1739-1746. doi: 10.1161/ATVBAHA.119.312461. Epub 2019 Aug 21. PMID: 31433698; PMCID: PMC6709697.
[2] Osekowski M, Trytell A, La Gerche A, Prior D, MacIsaac A, Paratz ED. A Comprehensive Approach to Managing Methamphetamine-Associated Cardiomyopathy. Am J Cardiovasc Drugs. 2022 Jul;22(4):385-393. doi: 10.1007/s40256-022-00523-y. Epub 2022 Feb 14. PMID: 35157254.
[3] Schürer, Stephan et al. “Clinical Characteristics, Histopathological Features, and Clinical Outcome of Methamphetamine-Associated Cardiomyopathy.” JACC. Heart failure vol. 5,6 (2017): 435-445. doi:10.1016/j.jchf.2017.02.017
Info sull'autore